

![]()
Juan-Carlos Maldonado (1)
![]()
![]()
Este artículo está bajo una licencia de Creative CommonsAttribution-
NonCommercial-NoDerivs
3.0 Unported License
![]()
1 Médico; Farmacoepidemiólogo. Unidad de Farmaco- logía, Centro de Biomedicina; Cátedra de Farmacología, Escuela de Medicina, Universidad Central del Ecuador. Cátedra de Terapéutica Médica, Escuela de Medicina, Universidad de las Américas.
Correspondencia:
Dr. Juan-Carlos Maldonado
![]()
Recibido: 02 – Agosto – 2011
Aceptado: 30 – Agosto – 2011
![]()
Palabras clave: Heparina de bajo peso molecu- lar, Uso terapéutico, Eficacia, Reacciones adver- sas, Análisis de costo, Farmacología, Revisión.
Resumen
Las distintas heparinas de bajo peso molecular (HBPM) disponibles en terapéutica tienen un mecanismo de acción similar al de la heparina no fraccionada (HNF) pero con ventajas en el perfil farmacocinético. Diversos estudios han demostrado que las HBPM poseen una eficacia equivalente a la HNF para diversas indicaciones de uso, incluyendo prevención y tratamiento del tromboembolismo venoso, manejo del síndrome coronario agudo e infarto de miocardio. Algunas reacciones adversas como las complicaciones hemorrágicas y la trombocitopenia son menos frecuentes con las HBPM. Además, han mostrado tener una buena relación coste-efectividad en distintos escenarios clínicos. Es ra- zonable asumir que no existen grandes diferencias en eficacia y seguri- dad entre las distintas HBPM.
![]()
Abstract
Keywords: Low molecular weight heparin, Therapeutic use, Efficacy, Adverse effects, Cost analysis, Pharmacology, Review.
The various low-molecular-weight heparins (LMWHs) available for therapeutic use have mechanisms of action which are similar to the mechanisms of unfractionated heparin (UH) but with pharmacokinetic advantages. Various studies showed that LMWHs have equiva- lent efficacy when compared with UH, in a variety of settings, including prophylaxis and treatment of VTE disease, and management of acute coronary syndrome and myocar- dial infarction. Adverse drug reactions as hemorrhagic complications and heparin-indu- ced thrombocytopenia are less frequent with LMWHs. Moreover, LMWHs have a good cost-effectiveness in the clinical scenarios. It is reasonable to assume that there would not be large differences in efficacy and safety among different LMWHs.
Revista Médica Vozandes
Rev Med Vozandes 2012; 23: 61-70
![]()
61
![]()
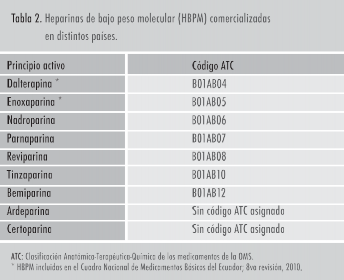
La clasificación Anatómica-Terapéutica-Química (ATC) de los medicamentos, desarrollada por el centro colaborador metodología estadística de la Organización Mundial de la Salud, organiza las distintas alternativas farmacológicas en niveles subsecuentes que logran diferenciar simultáneamen- te la estructura química, mecanismo de acción y los sistemas orgánicos que son blanco de los efectos terapéuticos [1]. En la misma, el nivel B01A corresponde al subgrupo fármaco- terapéutico de los agentes antitrombóticos (tabla 1), que incluye el subgrupo químico-terapéutico de las heparinas (B01AB) y a su vez en éste se encuentran contenidos en subniveles independientes de principios activos: la hepa- rina no fraccionada (HNF) en sus formas sódica y cálcica (B01AB01), la antitrombina III (B01AB02), las heparinas de bajo peso molecular (tabla 2) y los heparinoides (danapa- roide [B01AB09] y sulodexide [B01AB11]).
En este manuscrito se revisan los principales datos de efica- cia, seguridad, conveniencia y coste de las heparinas de bajo peso molecular.

62
![]()
Las heparinas de bajo peso molecular (HBPM) son sales de glucosaminoglucanos sulfatados con una masa molecular menor a 8000 daltons, las cuales se obtienen por fraccionamiento o despolimerización de la HNF. Al igual que la HNF, las HBPM ejercen su actividad anticoagulante por activación de la antitrombina III. Sin embar- go, a diferencia de la HNF (con actividad contra la trombina y el factor Xa) las HBPM muestran ac- tividad sobretodo contra el factor Xa debido a que las secuencias de pentasacaridos útiles para actuar existen en apenas el 15% a 25% de sus ca- denas. La potencia farmacológica de las HBPM se expresa en términos de unidades anti-factor Xa por miligramo [2-5]. En comparación con la HNF, las HBPM poseen un perfil farmacocinético más conveniente (tabla 3).
Las HBPM tienen como principal indicación de uso el manejo (profilaxis y tratamiento) del tromboem- bolismo venoso (trombosis venosa profunda [TVP] y tromboembolismo pulmonar [TEP]). En algunos países se ha autorizado el uso de enoxaparina, dalteparina y nadroparina como coadyuvantes del tratamiento para la angina inestable [2]. Ade- más, pueden ser utilizadas para prevenir la coa- gulación durante la hemodiálisis y otros procedi- mientos de circulación extracorpórea.
Las HBPM no están recomendadas para el uso en pacientes con válvulas cardiacas prostéticas ya que no ofrecen una adecuada profilaxis contra el tromboembolismo en esta condición, incluso cuando se emplean a dosis altas.
De las HBPM existentes (tabla 2), la dalteparina y enoxaparina constan como principios activos in- cluidos en la octava revisión (2010) del Cuadro Na- cional de Medicamentos Básicos del Ecuador [6].
![]()
![]()
Revista Médica Vozandes Volumen 23, Número 1, 2012
El tromboembolismo venoso (TEV) es una compli- cación frecuente en los pacientes hospitalizados, principalmente en aquellos sometidos a procedi- mientos quirúrgicos mayores. Su aparición puede conducir a embolismo pulmonar y muerte súbita. La prevención de estos cuadros es fundamental y puede ser realizada tanto con medidas mecá- nicas como farmacológicas. A pesar de que la importancia de la prevención del TEV está cla- ramente reconocida, generalmente ocurre una infrautilización de las alternativas [7–9].
Entre las alternativas farmacológicas disponibles para la prevención del TEV, las HBPM han demostrado sólidamen- te su eficacia y un favorable perfil de seguridad [10]. Entre los ensayos clínicos sobre este tema, dos de los más rele- vantes se han efectuado con enoxaparina y dalteparina. En este sentido, en el ensayo MEDENOX se asignó más de mil pacientes a dos brazos de tratamiento (enoxaparina dos regimenes [20 mg o 40 mg diarios por vía subcutánea] vs. placebo) administrados por 6 a 14 días. Los resultados mostraron que enoxaparina ofreció una reducción del 63% en el riesgo de TEV a los tres meses de seguimiento [11]. Por su parte, en el ensayo PREVENT se comparó en casi cuatro mil pacientes la eficacia de dalteparina (5000 UI diarias por vía subcutánea y por 14 días) contra placebo. A los tres meses de seguimiento, dalteparina logró reducir en un 44% el riesgo de TEV [12].
Considerando los estudios comparativos entre HBPM y HNF, inicialmente un metanálisis de nueve ensayos clínicos no logró identificar diferencias significativas entre ambos tipos de heparinas para la prevención de trombosis veno- sa profunda, embolismo pulmonar y mortalidad [13]. Sin em- bargo, posteriormente el ensayo clínico PREVAIL demostró que en los pacientes con enfermedad cerebrovascular isquémica, la terapia con enoxaparina era superior a la HNF para la prevención del TEV y que su uso podría ser preferible debido a la favorable relación beneficio/riesgo y mayor conveniencia [14].
Observaciones similares se han obtenido con fármacos de segunda generación. Por ejemplo, reviparina se ha mostrado más eficaz y mejor tolerada que la HNF para la prevención del TEV en cirugía general y ortopédica, mientras que en la prevención de recurrencias de la TVP posee más tolerabilidad en comparación con los anticoa- gulantes orales. En algunos trabajos comparativos contra enoxaparina, ha mostrado igual eficacia y aparentemen- te mejor perfil de seguridad [15].
En las indicaciones anteriores, nuevas alternativas an- titrombóticas tales como fondaparinux, rivaroxaban y dabigatran, han sido investigadas generalmente contra enoxaparina, una comparación que ha sido objeto de debate porque son fármacos que actúan en distintas fa- ses de la trombogenesis y poseen pautas de dosificación distintas [2, 16]. En este sentido, los nuevos antitrombóticos para alcanzar sus efectos máximos se administran en dosis cercanas a los límites de tolerancia, mientras que las HBPM poseen un mejor potencial de adaptabilidad posológica. Por otra parte, los nuevos anticoagulantes se han asociado con un mayor riesgo de sangrado, excediendo incluso en un 30% el descrito para enoxaparina [16]. La conveniencia de rivaroxaban y dabigatran en pacientes adultos mayores tampoco sería elevada, por cuanto tienden a mostrar una acumulación renal dependiente de la edad [2, 16].
Finalmente, en diversos ensayos clínicos conducidos en mujeres embarazadas, las HBPM han mostrado un perfil de seguridad favorable y franca eficacia para prevenir el TEV, así como un beneficio en la disminución del riesgo de otras complicaciones obstétricas asociadas con la trombo- filia, tales como pérdidas recurrentes, restricción del creci- miento fetal, preeclampsia, desprendimiento de placenta y muerte fetal intrauterina [17].
![]()
Varios ensayos clínicos han comparado la eficacia y seguridad de las HBPM en el tratamiento del TEV. Un trabajo que analizó sistemáticamente la litera- tura sobre el tema, incluyó un total de 101 artícu- los de los cuales al menos 17 fueron revisiones sis- temáticas. Conforme este trabajo, las HBPM más evaluadas fueron enoxaparina (en 13 revisiones sistemáticas), dalteparina (12 revisiones), nadro- parina (11 revisiones), tinzaparina (10 revisiones) y raviparina (9 revisiones). En general, existe una fuerte evidencia del beneficio clínico de las dis- tintas HBPM, aunque debido a una variabilidad metodológica importante entre las distintas inves- tigaciones es difícil efectuar análisis específicos [18].
Para el tratamiento de la trombosis venosa pro- funda (TVP), hace más de 10 años un metanálisis de 16 ensayos clínicos comparativos entre HBPM y HNF, ya reportó que las HBPM ofrecían una re- ducción del 49% en el riesgo de que ocurra una extensión del trombo. En el mismo estudio no existieron diferencias significativas entre los dos tipos de heparinas respecto a la disminución en el riesgo de recurrencias, hemorragias mayores y mortalidad total [19].
Posteriormente, otras revisiones sistemáticas han evaluado la eficacia de las HBPM (administradas a dosis fijas por vía subcutánea) en comparación de HNF (administrada a dosis ajustadas por vía subcutánea o intravenosa), para el tratamiento de la TVP [20, 21]. Uno de estos trabajos incluyó nue- ve ensayos clínicos (representando más de cua- tro mil pacientes) y reportó que en comparación con la HNF, las HBPM reducían significativamen- te la mortalidad total en un 38% luego de 3 a 6 meses de tratamiento; además, disminuían en un 43% la recurrencia de TEV sintomático, en un 37% la recurrencia de TVP sintomática y en un 58% el TEP [20]. Una segunda revisión más reciente, efec- tuó un análisis de 23 estudios abarcando datos de 9587 individuos y encontró resultados similares a favor de las HBPM [21]. En la misma indicación de uso, el empleo de nuevos anticoagulantes, tales como fondaparinux (un inhibidor selectivo del fac- tor Xa), no se han mostrado superiores a la enoxa- parina para el tratamiento inicial de la TVP [22].
En comparación con los anticoagulantes orales, una revisión sistemática de siete ensayos clínicos no encontró diferencias significativas entre las HBPM y esos fármacos para reducir la mortalidad o el TEV recurrente luego de tres meses de trata- miento [23]. Un resultado similar se observó en otro ensayo clínico con tinzaparina, luego de seis me- ses de tratamiento [24].
Para el tratamiento del embolismo pulmonar (TEP) la eficacia de las HBPM también ha sido evidenciada en varios estudios. Sin embargo
un metanálisis de 12 ensayos clínicos que incluyó estudios efectuados con enoxaparina, dalteparina, nadroparina, tinzaparina, reviparina y certoparina, no logró encontrar diferencias significativas en el beneficio al comparar las distintas HBPM con la HNF intravenosa [25]. Una revisión sis- temática en la cual se evaluaron distintas intervenciones terapéuticas para el manejo del TEV, también concluyó que las HBPM son modestamente superiores a la HNF en la prevención de la TVP recurrente e igual de eficaces para el tratamiento del TEP [18].
En subgrupos poblacionales especiales, los resultados obte- nidos en las investigaciones han sido en cierta forma pare- cidos a los anteriores. Así, en el tratamiento inicial del TEV en pacientes con cáncer, las HBPM se han reportado algo mejores que la HNF [26], mientras que comparadas contra los anticoagulantes orales para el tratamiento a largo plazo del TEV se las ha encontrado superiores para reducir el riesgo relativo de TEV recurrente, pero sin diferencias significativas para disminuir la mortalidad, las complicaciones hemorrá- gicas y la frecuencia de trombocitopenia [27, 28]. Utilizadas para el tratamiento del TEV durante el embarazo, las HBPM han mostrado un favorable perfil de eficacia y seguridad [29], aunque otros autores consideran que la evidencia disponi- ble podría requerir mayor confirmación debido a las varia- bilidades metodológicas entre los estudios realizados [17, 18].
Hace poco, el potencial beneficio de las HBPM en el síndro- me postrombótico fue reportado por una revisión sistemá- tica que logró identificar nueve estudios que recolectaron datos relacionados con esta complicación en pacientes bajo tratamiento prolongado luego de una TVP. En el aná- lisis ponderado se encontró una reducción del 87% en la in- cidencia de úlceras venosas a los tres meses de terapia con HBPM, siendo incluso superiores a los anticoagulantes orales en la recanalización completa de las venas trombosadas [30].
Para el manejo del síndrome coronario agudo (infarto agu- do de miocardio [IAM] sin elevación del segmento ST, IAM sin onda Q y angina inestable), algunos estudios han eva- luado el beneficio de añadir heparinas al tratamiento con antiagregantes plaquetarios. Entre las HBPM, la enoxapa- rina, dalteparina y nadroparina son las que han obtenido en algunos países autorización de uso para el tratamiento coadyuvante de la angina inestable [2]. Por su parte, la re- viparina ha sido aprobada para la prevención de eventos tromboticos agudos en pacientes sometidos a angioplastia coronaria transluminal percutánea [15].
Una revisión sistemática sobre siete ensayos clínicos contro- lados con placebo y conducidos en pacientes con angina inestable tratados con antiagregante plaquetario (ácido acetilsalicílico), encontró que la adición de HBPM logró re- ducir en un 66% el riesgo de mortalidad y de IAM durante el uso a corto plazo (primeros siete días), sin incrementar significativamente el riesgo de sangrado. Sin embargo, no hubo diferencias significativas con el tratamiento a largo plazo (hasta 3 meses) para los mismos desenlaces [31].
En la misma indicación de uso, otra revisión sistemática de ensayos clínicos conducidos sobre pacientes con angina inestable o IAM sin elevación del segmento ST, en los cuales se compararon HBPM contra HNF, reportó una disminución del 17% en el riesgo de IAM a favor de las HBPM. No obstan-
te, no logró encontrar diferencias significativas entre ambos tipos de tratamiento para reducir el riesgo de angina recurrente, mortalidad total o complicaciones hemorrágicas [32]. Comparadas entre sí como adyuvantes del tratamiento antia- gregante en la enfermedad coronaria, el ensayo clínico EVET reportó que enoxaparina tenía una eficacia superior a la tinzaparina tanto en el cor- to plazo (30 días de seguimiento) como a los seis meses de seguimiento, para reducir el riesgo de eventos isquémicos [33, 34].
Las HBPM también han sido evaluadas como tera- pia coadyuvante en el infarto agudo de miocardio. Así, en el ensayo clínico ASSENT-3 participaron cer- ca de seis mil pacientes y se evaluó la mortalidad a los 30 días de seguimiento. Los resultados mos- traron que enoxaparina añadida a la fibrinolisis re- ducía un 26% la frecuencia de nuevas complica- ciones isquémicas en comparación con la HNF [35].
Posteriormente, un ensayo clínico controlado en cerca de 20 mil pacientes portadores de IAM con elevación del segmento ST y sometidos a fibrinolisis de base, comparó dos brazos de tra- tamiento coadyuvante (enoxaparina vs. HNF) administrados durante las primeras 48 horas de manejo. Sus hallazgos mostraron que la enoxa- parina fue superior a la HNF, logrando reducir en un 17% el riesgo relativo de muerte o la recurren- cia de IAM en los primeros treinta días de segui- miento, pero que este beneficio se acompaño de un incremento significativo (2.1% vs. 1.4% res- pectivamente para los fármacos) en el riesgo de complicaciones hemorrágicas [36]. No obstante, recientemente un trabajo que utilizó un enfoque de análisis Bayesiano [37], sugirió que las HBPM po- drían formar parte de la primera línea de trata- miento para reperfusión coronaria. Este estudio analizó la información de 13 ensayos clínicos con HBPM (ocho contra HNF y cinco contra placebo) en pacientes con IAM con elevación del seg- mento ST. Los resultados indicaron una reducción del 21% (odds ratio= 0.79; IC95%= 0.67 – 0.94) en el riesgo considerando todos los estudios, pero sin diferencias en comparación con la HNF (odds ra- tio= 0.74; IC95%= 0.54 – 1.02); además, tampoco hubo un incremento significativo en el riesgo de eventos hemorrágicos [37].
Finalmente, se ha investigado a las heparinas como coadyuvantes del tratamiento de la colitis ulcerativa. Una nueva revisión sistemática en el tema comunicó que en esa indicación el benefi- cio es dudoso [38]. Conforme los hallazgos, la HNF es significativamente inferior a los corticosteroides y aumenta el riesgo de hemorragia rectal. A su vez, las HBPM por vía subcutánea no ofrecen ningún beneficio y si se administran en dosis altas formula- das en tabletas para liberación extendida en co- lon, son mejores que el placebo para lograr una remisión clínica (OR= 2.73; IC95%= 1.3 – 5.6) y alivio sintomatológico (2.25; 1.01 – 5.01), pero no para lograr una curación endoscópica o histológica.
![]() Intercambiabilidad entre HBPM
Intercambiabilidad entre HBPM
Varias HBPM han demostrado eficacia y seguridad equiva- lentes cuando se han comparado contra HNF intravenosa y contra HNF subcutánea a altas dosis, por lo cual es razo- nable asumir que no existien diferencias importantes en la eficacia y seguridad de los distintos principios activos.
A pesar de lo anterior, existen pocas comparaciones de HBPM entre sí y las pequeñas variaciones en las caracterís- ticas farmacodinámicas y farmacocinéticas que poseen, podrían conducir a ciertas diferencias en la eficacia clíni- ca y seguridad entre las distintas HBPM [39]. Esto se ha ob- servado ya con enoxaparina, dalteparina, nadroparina y tinzaparina en algunos escenarios clínicos [40, 41] y en subgru- pos específicos de pacientes, como por ejemplo sujetos con falla renal y con síndrome coronario agudo [33, 34, 42]. Po- tencialmente, este tipo de diferencias clínicas podrían ser más evidentes con el empleo de altas dosis y tratamientos
[39]
cativamente el riesgo de complicaciones hemorrá- gicas mayores en comparación con la frecuencia provocada por HNF [20]. En otra revisión sistemáti- ca que comparó las HBPM con anticoagulantes orales, se encontró que las primeras reducen las complicaciones hemorrágicas mayores (dis- minución del riesgo relativo del 42%) durante la terapia a largo plazo. Sin embargo, en la misma revisión se efectuó un análisis independiente de los ensayos clínicos que lograron mantener ocul- to de mejor forma el proceso de asignación a los tratamientos y la evaluación de los distintos des- enlaces. Considerando sólo esos estudios, no se encontró diferencias significativas entre las HBPM y los anticoagulantes orales [23].
En pacientes con IAM sin elevación del segmento ST, un metanálisis comparativo entre enoxaparina y HNF reportó que no había diferencias entre los dos tipos de tratamiento en cuanto el riesgo de sangra-
prolongados , generalmente utilizados con fines de trata-
miento antes que para prevención.
Lo anterior obedece a que las potencias de expresión an- titrombóticas difieren entre HBPM específicas. En este sen- tido, la potencia de las HBPM se encuentra expresada en términos de unidades anti-factor Xa por miligramo y la razón entre la actividad anti-factor Xa y anti-factor IIa. Esta razón (Xa/IIa) difiere para cada HBPM y ninguna de ellas puede ser utilizada de forma intercambiable unidad por unidad [2–4].
Aunque los estudios conducidos en modelos animales han aportado alguna información respecto a la eficacia anti- trombótica comparada de HBPM entre ellas, los resultados no son directamente aplicables a la trombosis en humanos. Desafortunadamente ese tipo de evaluaciones específicas no se han realizado porque la ejecución de ensayos clíni- cos con un número suficiente de sujetos son complejos me- todológicamente y costosos [4].
Por lo tanto, varios autores coinciden en que si bien la evi- dencia actual sugiere que las HBPM ofrecen resultados clí- nicos similares, existe una falta de bioequivalencia entre los distintos principios activos y no es posible considerar a las
[4, 15, 39, 40, 43]
do a corto plazo [44]. Sin embargo, otros autores han comunicado que si se modifican los criterios para clasificar las complicaciones hemorrágicas en en- sayos clínicos conducidos sobre pacientes con síndrome coronario agudo, podría existir un mayor riesgo en los pacientes tratados con HBPM [45].
Debido a que las HBPM tienen el potencial de acumularse en pacientes con disminución de la función renal, podrían asociarse con un mayor riesgo de sangrado. Un metanálisis al respecto que incluyó 18 estudios comunicó que la enoxa- parina utilizada a dosis habituales en pacientes con insuficiencia renal, incrementa entre dos a tres veces el riesgo de hemorragia, por lo cual podría ser necesario efectuar ajustes en la dosi- ficación del fármaco. Lamentablemente, este trabajo no pudo emitir conclusiones adecuadas respecto a otras HBPM, porque mientras para enoxaparina la información fue suficiente (15 es- tudios disponibles), para tinzaparina (2 estudios) y dalteparina (un estudio) la evidencia científi- ca fue deficiente [42]. El riesgo de esta compli- cación en pacientes con falla renal también
HBPM intercambiables entre ellas .
![]() Seguridad clínica de las HBPM
Seguridad clínica de las HBPM
Los efectos indeseados reportados con las diferentes HBPM son similares a los identificados con la HNF. Aunque ocurren con una menor frecuencia, las principales reacciones adver- sas descritas para todas las HBPM incluyen principalmente: hemorragia, trombocitopenia y otras reacciones alérgicas, irritación en el sitio de inyección, aparecimiento de nódulos inflamatorios, osteoporosis, hipercalemia y elevación en las pruebas funcionales hepáticas [2].
Algunas revisiones sistemáticas también han evaluado la se- guridad comparada de las HBPM, sobretodo en los dos prin- cipales efectos indeseados: hemorragia y trombocitopenia. Uno de estos trabajos identificó que las HBPM reducen signifi-
se ha descrito con la HNF [46], mientras que los nuevos antitrombóticos podrían conllevar un riesgo elevado particularmente en pacientes de tercera edad [16] y las complicaciones he- morrágicas de algunos pueden ser mayores comparados con las HBPM.
Se conoce que todas las heparinas en general pueden desencadenar reacciones de hipersensibi- lidad. Con las HBPM estos efectos indeseados pue- den manifestarse como urticarias, posiblemente por liberación local de histamina; o con las característi- cas clásicas de una reacción tipo I de aparecimien- to inmediato. De mayor severidad son la necrosis cutánea debida a vasculitis (reacción de Arthus tipo III) o la trombocitopenia. Lesiones eritematosas bien circunscritas y sin necrosis, son generalmente secundarias a reacciones tardías tipo IV. Todos estos cuadros no dependen del mecanismo de acción y por lo tanto son impredecibles en los pacientes [2].
La trombocitopenia es una de las reacciones adversas más peligrosas. Su fisiopatología no se comprende totalmente, pero se conoce que obedece a la formación de anticuer- pos contra el factor 4 del complejo heparino-plaquetario lo- calizado en la superficie de la plaqueta. Respecto al riesgo para desarrollar el cuadro, en una revisión sistemática no se encontró diferencia significativa entre las HBPM y la HNF [47]. Algo similar se observó en un ensayo clínico que comparó tres esquemas de tratamiento (HBPM por 5 a 7 días, HBPM hasta por 30 días y HNF por 5 a 7 días), donde la frecuen- cia de trombocitopenia a largo plazo no fue diferente en- tre los dos tipos de heparinas [48]. Estos datos contradicen la


teoría de que el peso molecular sería el principal determinante de la reacción, originada por una hi- persensibilidad impredecible. En los pacientes que desarrollan anticuerpos y trombocitopenia, podría ser preferible el empleo de antitrombóticos que po- sean otros mecanismos de acción, como por ejem- plo inhibidores de la trombina.
Por otra parte, se ha postulado que el peso mole- cular podría ser un factor importante en las reac- ciones retardadas y en la posibilidad de reacciones alérgicas cruzadas. Una reciente revisión de las pu- blicaciones sobre este problema, comunicó que la probabilidad de presentar reacciones cruzadas es mayor luego de una reacción tardía a HNF an- tes que a HBPM y que el peso no se correlaciona con el riesgo, por lo cual cada fármaco debería ser considerado por separado. Aparentemente, el fondaparinux conlleva una baja frecuencia de hi- persensibilidad, por lo cual sería la mejor alternativa cuando en un paciente existen antecedentes de reacciones alérgicas tardías [49].
![]() Conveniencia de uso de las HBPM
Conveniencia de uso de las HBPM
Como clase farmacológica las HBPM poseen un perfil farmacocinético que es más predecible al de la HNF. Ofrecen una mayor biodisponibilidad, menor afinidad para unirse a proteínas y una se- mivida biológica más larga que la HNF; además, pueden ser administradas una o dos veces diarias por vía subcutánea, de forma intradomiciliaria, sin que se requiera efectuar un monitoreo en las cifras de anticoagulación o ajustar regularmente su dosificación; (tabla 3). Por todo esto, su con- veniencia es mayor a la de HNF [3, 5, 50]. Aunque el esquema de tratamiento consistente en una ad- ministración diaria no se ha demostrado diferen- te al empleo de dos dosis diarias, podría implicar una mayor probabilidad de falla terapéutica [51]. Las contraindicaciones e interacciones farmaco- lógicas de las HBPM son similares a las existentes para la HNF [2].
Las dosis recomendadas (fijas en unidades anti-Xa o ajustadas en unidades/kg) para la prevención del TEV son diferentes para cada HBPM, aunque tienen como aspecto común que para pacientes (quirúrgicos o ingresados en servicios clínicos) con riesgo moderado de TEV se utilizan dosis más bajas, mientras que las dosis son mayores para pacientes con riesgo elevado de TEV sometidos a cirugía general u ortopédica; (tabla 4). Su administración puede iniciar 12 horas antes del procedimiento y seguir en el postoperatorio por 7 a 10 días o incluso pro-
longarse más en caso necesario. Las dosis utilizadas para el tratamiento del TEV y para la angina inestable, son mayores a las utilizadas en la profilaxis y generalmente ajustadas se- gún el peso corporal de la persona [2, 3, 7, 50].
![]() Coste asociado al uso de HBPM
Coste asociado al uso de HBPM
Los gastos en salud asociados con el TEV pueden ser sig- nificativamente elevados [52]. Conforme los análisis farma- coeconómicos internacionales, el empleo adecuado de los anticoagulantes ofrece una favorable relación de efi- ciencia (entre el coste y el beneficio obtenido), principal- mente cuando se utilizan en pacientes con riesgo elevado de TEV [53]. Además, también se ha comunicado que en situaciones donde existe un fármaco anticoagulante más costoso, éste solamente es más costo-efectivo (en relación a otros tipos de anticoagulantes) si se encuen- tra claramente demostrado que es más eficaz o que re- duce substancialmente otros costes directos e indirectos del tratamiento [53, 54].
En el caso de las HBPM, la evidencia actual sugiere que como clase farmacológica ofrecen resultados clínicos si- milares, pero por diferencias puntuales farmacodinámicas/ farmacocinéticas y la insuficiente información de estudios comparativos (que confirmen o descarten claramente la superioridad de alguna), no se las puede considerar inter- cambiables entre ellas [4, 39, 40, 43]. En este sentido, la aproxi- mación farmacoeconómica con diseño minimización de costes (aplicable cuando las alternativas terapéuticas po- seen igual eficacia), no es la más apropiada para compa- rar las distintas HBPM. De ahí que generalmente han sido evaluadas como clase farmacológica contra otras alter-
Revista Médica Vozandes
nativas antitrombóticas, mediante diseños de coste-efectividad. En ese tipo de trabajos se ha reconocido que aunque las HBPM son productos farmacéuticos más costosos que la HNF, logran ofrecer una mejor relación coste-efectividad [18, 54].
Una revisión sistemática de varios estudios far- macoeconómicos y metanálisis, en los cuales se había comparado la relación coste-efectividad de HNF y las HBPM (enoxaparina, nadroparina, tinzaparina y dalteparina), reportó que éstas últi- mas son la mejor alternativa cuando se tiene en cuenta dentro del análisis a su conveniencia y las posibilidades de uso en subgrupos particulares de pacientes [54].
La relación de eficiencia a favor de las HBPM se ha apreciado para la prevención del TEV hospi- talario [55], el tratamiento del TEP [56] y el tratamien- to a largo plazo del TEV en pacientes ambula- torios que habrían merecido como alternativa anticoagulantes orales [57]. Adicionalmente, la posibilidad de conseguir altas hospitalarias más tempranas en pacientes tratados con HBPM, también representaría un ahorro adicional en los costes de salud [54, 56].
Algo similar se ha descrito en estudios farma- coeconómicos publicados para enoxaparina y otras HBPM, las cuales se han mostrado más cos- to-efectivas que la HNF para reducir el costo total de cuidados de salud cuando se las utiliza para la prevención del TEV en pacientes hospitalizados con riesgo elevado [58, 59].
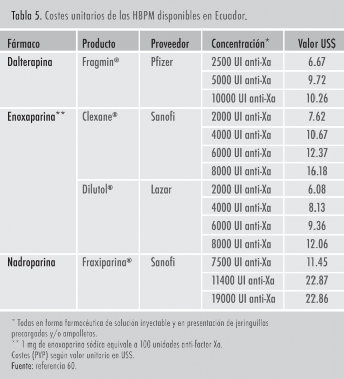
En el mercado ecuatoriano se han registrado y comercializado al menos tres HBPM [60], con un rango de costes unitarios comprendido entre US$ 6 y US$ 22; (tabla 5). Dos (dalteparina y enoxapa- rina) forman parte del Cuadro Nacional de Me- dicamentos Básicos [6]. Conforme a la evidencia científica revisada, el perfil de eficacia, seguridad y conveniencia sería similar para todas ellas, así como su relación coste-efectividad al emplearlas en la práctica clínica habitual.
![]() Conflictos de interés
Conflictos de interés
JCM ha cumplido actividades como consultor para el Consejo Nacional de Salud y la Comisión Nacional de Medicamentos Básicos, en procesos relacionados con la revisión del Cuadro Nacional de Medicamentos Básicos y su Registro Terapéuti- co. Además, es consultor del Comité de Bioética de la Universidad Central del Ecuador, para la eva- luación de ensayos clínicos con medicamentos.
67
Maldonado JC.
Heparinas de bajo peso molecular: revisión de la evidencia en sus principales indicaciones de uso

![]() Presentaciones previas
Presentaciones previas
Un análisis similar de la evidencia científica disponible para las HBPM fue realizado por el autor en el marco de una consultoría técnica:
Maldonado JC. Subgrupo químico de la heparina (B01AB) – Heparinas de bajo peso molecular. Informe sobre principios activos que pueden ser incluidos en los espacios dejados solamente para el subgrupo químico tera- péutico. Consultoría Técnica de apoyo en la revisión del Cuadro Nacional de Medicamentos Básicos. Quito: Consejo Nacional de Salud; 2008.
![]()
7.
6.
5.
3.
4.
2.
1.
WHO Collaborating Centre for Drug Statis- tics Methodology. ATC classification and DDD assignment. Oslo: WHO Collabora- ting Centre for Drug Statistics Methodo- logy, 2011. [Disponible en: http://www. whocc.no/atcddd/].
Sweetman SC, ed. Martindale – The com- plete drug reference. Thirty-fifth edition. London: Pharmaceutical Press, 2007.
Weitz JI. Low-molecular-weight-heparins. N Engl J Med 1997; 337: 688-99.
Morris TA. Heparin and low molecular weight heparin: background and phar- macology. Clin Chest Med 2003; 24: 39-47.
Nutescu EA, Shapiro NL, Chevalier A, Amin AN. A pharmacologic overview of current and emerging anticoagulants. Clev Clin J Med 2005; 72 (Supp 1): S2–S6.
Comisión Nacional de Medicamentos e Insumos. Cuadro Nacional de Medica- mentos Básicos y Registro Terapéutico. Octava Revisión 2010. Quito: Consejo Na- cional de Salud, 2010.
National Collaborating Centre for Acu- te and Chronic Conditions. NICE clinical guideline 92: Reducing the risk of venous thromboembolism (deep vein thrombosis and pulmonary embolism) in patients ad-
mitted to hospital. London: National Ins- titute for Health and Clinical Excellence; 2010.
8.
9.
10.
11.
12.
Jaffer AK. An overview of venous throm- boembolism: Impact, risk, and issues in prophylaxis. Clev Clin J Med 2008; 75 (Supp 3): S3–S6.
Cohen AT, Tapson VF, Bergmann JF, Gol- dhaber SZ, Kakkar AK, Deslandes B, et al; for the ENDORSE investigators. Venous thromboembolism risk and prophylaxis in the acute hospital care setting (ENDORSE study): a multinational cross-sectional stu- dy. Lancet 2008; 371: 387-94.
Jaffer AK, Amin AN, Brotman DJ, Deitel- zweig SB, McKean SC, Spyropoulos AC. Prevention of venous thromboembolism in the hospitalized medical patient. Clev Clin J Med 2008; 75 (Supp 3): S7–S16.
Samama MM, Cohen AT, Darmon JY, Desjardins L, Eldor A, Janbon C, et al., for the Prophylaxis in Medical Patients with Enoxaparin Study Group. A comparison of enoxaparin with placebo for the preven- tion of venous thromboembolism in acu- tely ill medical patients. N Engl J Med 1999; 341: 793-800.
Leizorovicz A, Cohen AT, Turpie AG, Olsson CG, Vaitkus PT, Goldhaber SZ; for the PRE-
VENT Medical Thromboprophylaxis Study Group. Randomized, placebo controlled trial of dalteparin for the prevention of venous thromboembolism in acutely ill medical patients. Circulation 2004; 110:
13.
14.
15.
16.
874–879.
Mismetti P, Laporte-Simitsidis S, Tardy B, Cucherat M, Buchmüller A, Juillard-Delsart D, et al. Prevention of venous thromboem- bolism in internal medicine with unfractio- nated or low-molecular weight heparins: a meta-analysis of randomised clinical trials. Thromb Haemost 2000; 83: 14–19.
Sherman DG, Albers GW, Bladin C, Fieschi C, Gabbai AA, Kase CS, et al., on behalf of the PREVAIL Investigators. The efficacy and safety of enoxaparin versus unfrac- tionated heparin for the prevention of venous thromboembolism after acute is- chaemic stroke (PREVAIL Study): an open- label randomised comparison. Lancet 2007; 369: 1347-55.
Del Bono R, Martini G, Volpi R. Update on low molecular weight heparins at the be- ginning of third millennium. Focus on revi- parin. Eur Rev Med Pharmacol Sci 2011; 15: 950 - 59.
Welzel D, Hull R, Fareed J. Prophylaxis of venous thromboembolism: low molecular weight heparin compared to the selective
17.
18.
19.
20.
21.
22.
23.
24.
25.
26.
27.
28.
29.
30.
31.
32.
33.
34.
35.
36.
37.
38.
39.
40.
41.
42.
43.
44.
45.
46.
47.
anticoagulants rivaroxaban, dabigatran and fondaparinux. Int Angiol 2011; 30: 199 - 211.
D’Ippolito S, Ortiz AS, Veglia M, Tersigni C, Di Simone N. Low molecular weight hepa- rin in obstetric care: a review of the litera- ture. Reprod Sci 2011; 18: 602 - 13.
Segal JB, Streiff MB, Hofmann LV, Thornton K, Bass EB. Management of venous throm- boembolism: A systematic review for a practice guideline. Ann Intern Med 2007; 146: 211-22.
Leizorovicz A, Simonneau G, Decousus H, Boissel JP. Comparison of efficacy and safety of low molecular weight hepa- rins and unfractionated heparin in initial treatment of deep venous thrombosis: a meta-analysis. BMJ 1994; 309: 299-304.
investigators. Low-molecular-weight he- parin versus a coumarin for the prevention of recurrent venous thromboembolism in patients with cancer. N Engl J Med 2003; 349: 146-53.
Akl EA, Barba M, Rohilla S, Terrenato I, Spe- rati F, Muti P, et al. Low-molecular-weight heparins are superior to vitamin K antago- nists for the long term treatment of venous thromboembolism in patients with cancer: a Cochrane Systematic Review. Journal of Experimental & Clinical Cancer Research 2008; 27: 21.
Greer IA, Nelson-Piercy C. Low-molecular- weight heparins for thromboprophylaxis and treatment of venous thromboembolism in pregnancy: a systematic review of safety and efficacy. Blood 2005; 106: 401-07.
tion: a Bayesan approach. Eur Rev Med Pharmacol Sci 2011; 15: 701 – 10.
Chande N, MacDonald JK, Wang JJ, Mc- Donald JW. Unfractionated or low mo- lecular weight heparin for induction of remission in ulcerative colitis: a Cochrane inflammatory bowel disease and functio- nal bowel disorders systematic review of randomized trials. Inflamm Bowel Dis 2011; 17: 1979 – 86.
Farred J, Walenga JM. Why differentiate low molecular weight heparins for venous thromboembolism? Thrombosis Journal 2007; 5: 8.
Nenci G. Low molecular weight heparins: are they interchangeable? No. J Thromb Haemost 2003; 1: 12-13.
van Dongen CJ, van den Belt AG, Prins MH, Lensing AW. Fixed dose subcutaneous low molecular weight heparins versus ad- justed dose unfractionated heparin for venous thromboembolism. Cochrane Da- tabase Syst Rev 2004; (4): CD001100.
Erkens PM, Prins MH. Fixed dose subcuta- neous low molecular weight heparins ver- sus adjusted dose unfractionated heparin for venous thromboembolism. Cochrane Database Syst Rev 2010; (9): CD001100.
Büller HR, Davidson BL, Decousus H, Gallus A, Gent M, Piovella F, et al., for the Matisse Investigators. Fondaparinux or enoxaparin for the initial treatment of symptomatic deep venous thrombosis. A randomized trial. Ann Intern Med 2004; 140: 867-73.
van der Heijden JF, Hutten BA, Büller HR, Prins MH. Vitamin K antagonists or low- molecular-weight heparin for the long term treatment of symptomatic venous thromboembolism. Cochrane Database Syst Rev 2002; (1): CD002001.
Daskalopoulos ME, Daskalopoulou SS, Tzortzis E, Sfiridis P, Nikolaous A, Dimitrou- lis D, et al. Long-term treatment of deep venous thrombosis with a low molecular weight heparin (tinzaparin): a prospective randomized trial. Eur J Vasc Endovasc Surg 2005; 29: 638–50.
Quinlan DJ, McQuillan A, Eikelboom JW. Low-molecular-weight heparin compared with intravenous unfractionated heparin for treatment of pulmonary embolism. A meta-analysis of randomized, controlled trials. Ann Intern Med 2004; 140: 175-83.
Akl EA, Vasireddi SR, Gunukula S, Barba M, Sperati F, Terrenato I, et al. Anticoagu- lation for the initial treatment of venous thromboembolism in patients with cancer. Cochrane Database Syst Rev 2011; (2): CD006649.
Lee AYY, Levine MN, Baker RI, Bowden C, Kakkar AK, Prins M, et al., for the randomi- zed Comparison of Low-molecular-weight heparin versus Oral Therapy for the pre- vention of recurrent venous thromboe- mbolism in patients with cancer (CLOT)
Revista Médica Vozandes
Hull RD, Liang J, Townshend G. Long-term low-molecular-weight heparin and the post-thrombotic syndrome: a systematic review. Am J Med 2011; 124: 756-65.
Eikelboom JW, Anand SS, Malmberg K, Weitz JI, Ginsberg JS, Yusuf S. Unfractiona- ted heparin and low molecular weight he- parin in acute coronary syndrome without ST elevation: a meta-analysis. Lancet 2000; 355: 1936–42.
Magee KD, Sevcik W, Moher D, Rowe BH. Low molecular weight heparins versus un- fractionated heparin for acute coronary syndromes. Cochrane Database Syst Rev 2003; (1): CD002132.
Michalis LK, Katsouras CS, Papamichael N, Adamides K, Naka KK, Goudevenos J, et al. Enoxaparin versus tinzaparin in non- ST-segment elevation acute coronary syn- dromes: the EVET trial. Am Heart J 2003; 146: 304-10.
Katsouras CS, Michalis LK, Papamichael N, Adamides K, Naka KK, Nikas D, et al. Enoxaparin versus tinzaparin in non-ST- segment elevation acute coronary syn- dromes: results of the enoxaparin versus tinzaparin (EVET) trial at 6 months. Am Heart J 2005; 150: 385-91.
The Assessment of the Safety and Efficacy of a New Thrombolytic regimen (ASSENT)-3 Investigators. Efficacy and safety of te- necteplase in combination with enoxapa- rin, abciximab, or unfractionated heparin: the ASSENT-3 randomised trial in acute myocardial infarction. Lancet 2001; 358:
605-13.
Antman EM, Morrow DA, McCabe CH, Murphy SA, Ruda M, Sadowski Z, et al., for the ExTRACT-TIMI 25 Investigators. Enoxa- parin versus unfractionated heparin with fibrinolysis for ST-elevation myocardial in- farction. N Engl J Med 2006; 354: 1477–88.
Buccelletti E, Spadaccio C, Chello M, Mar- siliani D, Carroccia A, Iacomini P, Calabrò G, Gentiloni Silveri N, Franceschi F. A cri- tical review of the efficacy and safety in the use of low-molecular-weight heparin in acute ST-elevation myocardial infarc-
Simonneau G, Laporte S, Mismetti P, Der- lon A, Samii K, Samama CM, et al. A ran- domized study comparing the efficacy and safety of nadroparin 2850 IU (0.3 mL) vs. enoxaparin 4000 IU (40 mg) in the pre- vention of venous thromboembolism after colorectal surgery for cancer. J Thromb Haemost 2006; 4:1693-700.
Lim W, Dentali F, Eikelboom JW, Crowther MA. Meta-analysis: Low-molecular-weight heparin and bleeding in patients with se- vere renal insufficiency. Ann Intern Med 2006; 144: 673-84.
Jeske WP, Walenga JM, Hoppensteadt DA, Vandenberg C, Brubaker A, Adiguzel C, et al. Differentiating low-molecular- weight heparins based on chemical, biological, and pharmacologic proper- ties: implications for the development of generic versions of low-molecular-weight heparins. Semin Thromb Hemost 2008; 34:
74-85.
Petersen JL, Mahaffey KW, Hasselblad V, Antman EM, Cohen M, Goodman SG, et al. Efficacy and bleeding complications among patients randomized to enoxapa- rin or unfractionated heparin for antithrom- bin therapy in non-ST segment elevation acute coronary syndromes: a systematic overview. JAMA 2004; 292: 89-96.
Crowther MA, Warkentin TE. Bleeding risk and the management of bleeding com- plications in patients undergoing anticoa- gulant therapy: focus on new anticoagu- lant agents. Blood 2008; 111: 4871-79.
Thorevska N, Amoateng-Adjepong Y, Sa- bahi R, Schiopescu I, Salloum A, Muralid- haran V, et al. Anticoagulation in hospi- talized patients with renal insufficiency: a comparison of bleeding rates with unfrac- tionated heparin vs enoxaparin. Chest 2004; 125: 856-63.
Dolovich LR, Ginsberg JS, Douketis JA, Holbrook AM, Cheah G. A meta-analysis comparing low-molecular-weight hepa- rins with unfractionated heparin in the treatment of venous thromboembolism: examining some unanswered questions regarding location of treatment, product
69
48.
49.
50.
51.
type, and dosing frequency. Arch Intern Med 2000; 160: 181-88.
Lindhoff-Last E, Nakov R, Misselwitz F, Breddin HK, Bauersachs R. Incidence and clinical relevance of heparin-induced an- tibodies in patients with deep vein throm- bosis treated with unfractionated or low- molecular-weight heparin. Br J Haematol 2002; 118: 1137–1142.
Weberschock T, Meister AC, Bohrt K, Sch- mitt J, Boehncke WH, Ludwig RJ. The risk for cross-reactions after a cutaneous de- layed-type hypersensitivity reaction to he- parin preparations is independent of their molecular weight: a systematic review. Contact Dermatitis 2011; 65: 187 – 94.
Hirsh J, Bauer KA, Donati MB, Gould M, Samama MM, Weitz JI, for the American College of Chest Physicians. Parenteral Anticoagulants: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Edition). Chest 2008; 113 (6 Suppl): 141S-159S.
van Dongen CJ, MacGillavry MR, Prins MH. Once versus twice daily LMWH for the
initial treatment of venous thromboembo- lism. Cochrane Database Syst Rev 2005; (3): CD003074.
52.
53.
54.
55.
Tilleul P, LaFuma A, Colin X, Ozier Y. Esti- mated annual costs of prophylaxis and treatment of venous thromboembolic events associated with major orthopedic surgery in France. Clin Appl Thromb He- most 2006; 12: 473-84.
Fang MC, Minichiello T, Auerbach AD. Cost considerations surrounding current and future anticoagulant therapies. Cleve Clin J Med 2005; 72 (Suppl 1): S43-49.
Ward A, Getsios D, O’Brien J, Caro JJ. Economic assessments of low molecular weight heparin in venous thromboem- bolism. Expert Rev Pharmacoeconomics Outcomes Res 2004; 4: 39-74.
Wilbur K, Lynd LD, Sadatsafavi M. Low- molecular-weight heparin versus unfrac- tionated heparin for prophylaxis of venous thromboembolism in medicine patients--a pharmacoeconomic analysis. Clin Appl Thromb Hemost 2011; 17: 454-65.
Aujesky D, Smith KJ, Cornuz J, Roberts MS. Cost-effectiveness of low-molecular- weight heparin for treatment of pulmo- nary embolism. Chest 2005; 128: 1601-10.
56.
57.
58.
59.
60.
Santamaría A, Juárez S, Reche A, Gó- mez-Outes A, Martínez-González J, Font- cuberta J; ESFERA Investigators. Low- molecular-weight heparin, bemiparin, in the outpatient treatment and secondary prophylaxis of venous thromboembolism in standard clinical practice: the ESFERA Study. Int J Clin Pract 2006; 60: 518-25.
Hawkins D. Pharmacoeconomics of thrombosis management. Pharmacothe- rapy 2004; 24 (7 Pt 2): 95S – 99S.
Lynd LD, Goeree R, Crowther MA, O’Brien BJ. A probabilistic cost-effectiveness analy- sis of enoxaparin versus unfractionated heparin for the prophylaxis of deep-vein thrombosis following major trauma. Can J Clin Pharmacol 2007; 14: e215 - e226.
Vademecum Farmacoterapéutico del Ecuador 2011. Tercera edición. Quito: Sociedad Ecuatoriana de Medicina Fami- liar; 2011.
70